Hemoglobina jest białkiem złożonym z grupy prostetycznej zwanej hemem i białka globiny. Rozbudowany układ czterech pierścieni pirolowych połączonych mostkami metanowymi wykazuje silną absorbcję światła w zakresie 405-410 nm. Transportowanie tlenu przez hemoglobinę polega na utlenowaniu hemu. Z punktu widzenia chemii tlen tworzy wiązanie koordynacyjne pomiędzy żelazem (Fe+2) a histydyną. Reakcji tej towarzyszy zmiana konformacji cząsteczki. W warunkach niskiego ciśnienia parcjalnego tlenu w głębi tkanek i większego stężenia jonów wodorowych H+ dochodzi do odczepienia tlenu. Obie formy utlenowana i nieutlenowana zdecydowanie różnią się barwą – co spowodowane jest różnicami w pochłanianiu światła w zakresie 540 - 565 nm. Inne modyfikacje hemu także znajdują odbicie w sposobie pochłaniania światła. Żelazo w cząsteczce hemu pod wpływem czynników utleniających np. cyjanożelazian III potasu ulega utlenieniu do Fe+3 i traci zdolność transportu tlenu. Pochodna ta nosi nazwę methemoglobiny i charakteryzuje się dodatkowym maksimum pochłaniania światła w zakresie ok 630 nm. Zwiększenie stężenia methemoglobiny obserwuje się w przypadku zatrucia pestycydami chloroorganicznymi. Duże znaczenie dla diagnostyki ma analiza widma hemoglobiny w przypadku zatrucia tlenkiem węgla. Tlenkowęglowy hem nie ulega zmianom pod wpływem dodanego wodorosiarczynu sodu - co pozwala odróżnić hemoglobinę tlenkoweglową od nieuszkodzonej. Osoby zdrowe mają poniżej 1% HbCO, lecz u osób palących papierosy i u zawodowych kierowców wartość ta może wzrosnąć do 10%. Przy osiągnięciu poziomu 20% hemoglobiny HbCO występują objawy zatrucia. Analiza widma hemoglobiny ma także znaczenie w kryminalistyce: dzięki niej można wykryć zatrucia cyjankiem i określić przyczynę śmierci w pożarze.
Zjawisko absorpcji światła stanowi podstawę spektrofotometrii absorpcyjnej w nadfiolecie i w świetle widzialnym. Podstawowe prawo spektrofotometrii absorpcyjnej to prawo Lamberta-Beera, które wyraża się następująco:
A = ε c l
Gdzie:
Ɛ- molowy współczynnik absorpcji
c -stężenie substancji
l- długość drogi wiązki światła przez próbkę
Wykonanie ćwiczenia
1. Przygotować naczynia reakcyjne i podpisać je numerami 1-4, gdzie:
Nr 1- Szklana probówka
Nr 2- Eppendorf (2 ml)
Nr 3- Eppendorf (2 ml)
Nr 4- Szklana probówka
2. Próbkę 0,1 ml krwi przenieść do 10 ml wody destylowanej i odstawić na 10 minut. Po zakończeniu hemolizy roztwór odwirować lub przesączyć (opcjonalnie). Umieścić po 2 ml przygotowanego roztworu do probówek nr 1-4 (pozostałe 2 ml roztworu zostawić do ewentualnej powtórki analizy).
3. Zawartość probówki nr 1 natlenić przez energiczne wstrząsanie.
4. Do probówki nr 2 dodać 20 mg ditioninu sodu i wymieszać. Inkubować 15-30 minut w RT.
5. Do probówki nr 3 dodać 20 mg cyjanożelazianu III potasu i wymieszać. Inkubować 15-30 minut w RT.
6. Przez roztwór w probówce nr 4 przepuszczać strumień tlenku węgla (Rys. 1) otrzymany w reakcji kwasu mrówkowego ze stężonym kwasem siarkowym (UWAGA!!! Praca pod dygesorium!!!).
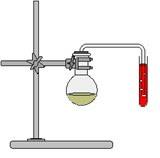
Rys. 1. Nasycanie roztworu tleniem węgla.
7. Dysponując gotowymi próbami różnych pochodnych hemoglobiny przygotować ich widma w zakresie 450-650 nm. Na podstawie uzyskanych widm określić długości fali, przy których występują maksima pochłaniania światła dla poszczególnych pochodnych hemoglobiny.
Beata Jarmołowska, Natalia Kordulewska










Komentarze
Prześlij komentarz